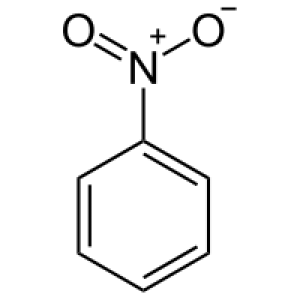
Нитробензол
Нитробензóл (нитробензéн, в просторечии — мирабáновое мáсло, мирабáновая эссéнция) — вещество класса нитроаренов.
Физические свойства
Внешний вид нитробензола — ярко-желтые кристаллы или маслянистая жидкость (бесцветная или зеленовато-жёлтая) с запахом горького миндаля, нерастворимая в воде (0,19 % по массе при 297 K, 0,8 % при 350 K). Растворяется в концентрированных кислотах (при разведении таких растворов водой осаждается). Неограниченно смешивается с диэтиловым эфиром, бензолом, некоторыми другими органическими растворителями. Перегоняется с водяным паром. Показатель преломления (для D-линии натрия (589 нм), при 297K) 1,5562. Дипольный момент газообразных молекул (в дебаях) 4,22 D. Удельная теплоёмкость 1,51 Дж/(г·К).
Химические свойства
Электрофильное замещение
В связи с сильным электроноакцепторным действием нитрогруппы реакции электрофильного замещения идут в мета-положение, и скорость реакции ниже чем у бензола.
- Нитрование. Образуется смесь изомеров: 93 % м-динитробензола, 6,5 % о-динитробензола и 0,5 % п-динитробензола.
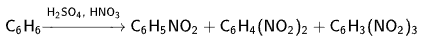
- Сульфирование
- Галогенирование
В присутствии катализаторов. Например, порошка железа:
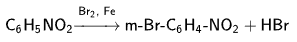
Не вступает в реакцию Фриделя-Крафтса.
Нуклеофильное замещение
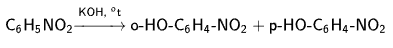
- При обработке магнийорганическими соединениями в эфире углеводородный радикал как нуклеофил вступает в орто- и в пара-положения к нитрогруппе (которая при этом восстанавливается до нитрозогруппы)
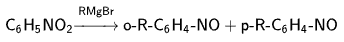
Восстановление
Наиболее важной реакцией ароматических нитросоединений является восстановление их до первичных аминов.
Эта реакция была открыта в 1842 году Н.Н. Зининым, который впервые восстановил нитробензол до анилина действием сульфида аммония:
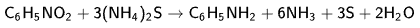
В настоящее время для восстановления нитрогруппы в аренах до аминогруппы в промышленных условиях применяется каталитическое гидрирование. В качестве катализатора используют медь на силикагеле. Катализатор готовят нанесением карбоната меди из суспензии в растворе силиката натрия и последующим восстановлением водородом при нагревании. Выход анилина над этим катализатором составляет 98 %.
Иногда в промышленном гидрировании нитробензола до анилина в качестве катализатора используют никель в комбинации с оксидами ванадия и алюминия. Такой катализатор эффективен в интервале 250—300° и легко регенерируется при окислении воздухом. Выход анилина и других аминов составляет 97—98 %. Восстановление нитросоединений до аминов может сопровождаться гидрированием бензольного кольца. По этой причине для получения ароматических аминов избегают использовать в качестве катализаторов платину, палладий или никель Ренея.
В промышленности анилин получают каталитическим восстановлением нитробензола на медном или никелевом катализаторе, который вытеснил старинный способ восстановления нитробензола чугунными стружками в водном растворе хлорного железа и соляной кислоты. Промежуточные продукты — нитрозобензол и N-фенилгидроксиламин.
Другой вариант получения нитрозобензола:
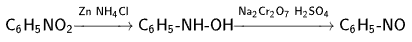
Восстановление нитрогруппы до аминогруппы сульфидом и гидросульфидом натрия в настоящее время имеет значение только для частичного восстановления одной из двух нитрогрупп, например, в м-динитробензоле или 2,4-динитроанилине.
При ступенчатом восстановлении полинитросоединений с помощью сульфида натрия этот неорганический реагент превращается в тетрасульфид натрия, что сопровождается образованием щелочи.
Высокая щелочность среды приводит к образованию азокси- и азо- и гидразосоединений в качестве побочных продуктов. Для того чтобы избежать этого в качестве восстановителя следует использовать гидросульфид натрия, где щелочь не образуется.
Азоксибензол может быть получен восстановлением нитробензола: спиртовым раствором едкого кали, амальгамой натрия, водородом в присутствии окиси свинца, метиловым спиртом и едким натром, метилатом натрия и метиловым спиртом, закисью свинца в щелочной суспензии, декстрозой в щелочной суспензии, β-фенилгидроксиламином.
Азобензол можно получить, например, восстановлением нитробензола при кипячении с цинковой пылью в водно-спиртовом растворе щёлочи.
Многие более восстановленные производные могут быть получены электрохимически, при правильном подборе электродов.
Известны методы восстановления нитросоединений до амидов (амальгамами натрия или цинка, сульфидами натрия и аммония).
Получение
Основной способ получения нитробензола (как и других нитроаренов) — нитрование в условиях электрофильного замещения бензола (соответственно, аренов). Электрофильной частицей является ион нитрония NO2.
В промышленности нитробензол получают непрерывным нитрованием бензола смесью концентрированных H2SO4 и HNO3 с выходом 96—99 %.
В лабораторных условиях нитробензол получают нитрованием бензола смесью H2SO4 (1,84 г/см3) и HNO3 (1,4 г/см3) в соотношении 1:1 при 40—60 °C (45 мин). Выход целевого продукта достигает 80 %.
Принципиально возможна (но не применяется в силу низкого выхода) реакция нитрования бензола концентрированной азотной кислотой.Несколько реже (как и для получения других нитроаренов) в лабораториях используют замещение, модификацию или элиминирование заместителей, уже имеющихся при бензольном кольце.
Например, возможно получать нитробензол окислением анилина перокситрифторуксусной кислотой (или другими окислителями; чем менее кислая среда — тем больше доля азоксибензола в продуктах).
Применение
Исходное сырьё в производстве анилина, ароматических азотсодержащих соединений (бензидин, хинолин, азобензол), растворитель эфиров целлюлозы, компонент полировальных составов для металлов. Применяется как растворитель и мягкий окислитель. В основном используется как прекурсор для производства анилина.
Производные нитробензола используются в качестве взрывчатых веществ и как компоненты ракетных топлив. В парфюмерии — в качестве душистых или фиксирующих запах веществ, в том числе — искусственных мускусов. Сам нитробензол ранее выпускали под названием «горько-миндального» или «мирабанового» масла. Некоторые производные нитробензола используются в составе лаков и красок. Некоторые применяются в медицине.
Биологическая роль и токсичность
Нитробензол токсичен: относится ко второму классу опасности и в больших концентрациях может вызывать гемолиз. Впитывается через кожу, оказывает сильное действие на ЦНС, нарушает обмен веществ, вызывает заболевания печени, окисляет гемоглобин в метгемоглобин.
ПДК в рабочей зоне — 1 мг/м³, ЛД50 — 120 мг/кг на крысах.