Ацетон
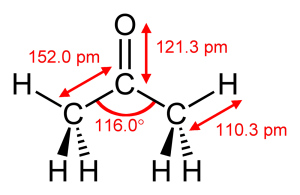
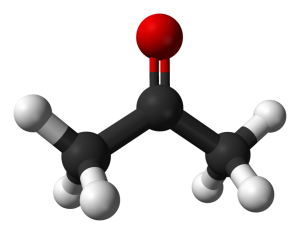
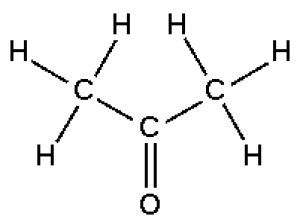
Ацето́н (пропано́н, димети́лкето́н, пропано́н-2, химическая формула — C3H6O или CH3-C(=O)-CH3) — органическое вещество, относящееся к классу насыщенных кетонов.
Бесцветная летучая жидкость с характерным запахом. Неограниченно смешивается с водой и полярными органическими растворителями, также в ограниченных пропорциях смешивается с неполярными растворителями.
Ацетон является ценным промышленным растворителем и, благодаря низкой токсичности, он получил широкое применение в производстве лаков, взрывчатых веществ, лекарственных средств. Он является исходным сырьем в многочисленных химических синтезах. В лабораторной практике его применяют в качестве полярного апротонного растворителя, для приготовления охлаждающих смесей вместе с сухим льдом и аммиаком, а также для мытья химической посуды.
Ацетон является одним из продуктов метаболизма в живых организмах, в частности, у человека. Он является одним из компонентов так называемых кетоновых тел, которых в крови здорового человека содержится крайне мало, однако при патологических состояниях (длительное голодание, тяжелая физическая нагрузка, тяжелая форма сахарного диабета) их концентрация может значительно повышаться и достигать 20 ммоль/л.
Происхождение названия
Своё название ацетон получил от лат. acetum — «уксус». Это связано с тем, что ранее ацетон получали из ацетатов, а из самого ацетона получали синтетическую ледяную уксусную кислоту. В 1848 году немецкий профессор медицины и химии Леопольд Гмелин ввёл термин в официальное употребление, использовав старое немецкое слово Aketon (кетон, ацетон), которое также берёт корни от латинского «acetum».
Открытие
Один из простейших и в то же время важнейших из кетонов — ацетон — впервые выявлен в 1595 году немецким химиком Андреасом Либавием в процессе сухой перегонки ацетата свинца. Однако точно определить его природу и химический состав удалось только в 1832 году Жану-Батисту Дюма и Юстусу фон Либиху. До 1914 года ацетон получали практически исключительно коксованием древесины, однако повышенный спрос на него в годы Первой мировой войны (для производства хлорацетона — эффективного слезоточивого вещества) очень быстро стимулировал создание новых методов производства.
Получение
Мировое производство ацетона составляет более 6,9 миллионов тонн в год (по данным на 2012 г.) и устойчиво растёт. В промышленности получается напрямую или косвенно из пропена.
Старые методы
Старейший метод промышленного производства ацетона заключался в сухой перегонке ацетата кальция, который образуется при нейтрализации известью древесного уксуса, который образуется при коксовании древесины.
Сейчас этот метод уже не применяется, так как ацетон в этом случае содержит слишком много примесей.
Известны также способы получения ацетона ацетоно-бутиловым брожением углеводов (крахмала, сахаров, меласса), вызываемым бактериями — клостридиями, в частности Clostridium acetobutylicum; в ходе брожения образуются ацетон и бутиловый или этиловый спирты. Ацетон и бутиловый спирт получают в мольном соотношении от 2:1 до 3:1. Метод характеризуется малыми выходами.
В Германии в 1916 г. был запатентован процесс производства ацетона на основе уксусной кислоты. При 400 °C через контакты из церия пропускали уксусную кислоту.
Ацетон также производили из ацетилена прямым синтезом. Ацетилен вступает во взаимодействие с водяным паром при 450 °C в присутствии катализаторов.
Кумольный способ
Основную часть ацетона получают как сопродукт при получении фенола из бензола по кумольному способу. Процесс протекает в 3 стадии.
На первой стадии бензол алкилируется пропеном с получением изопропилбензола (кумола), на второй и третьей (реакция Удриса — Сергеева) полученный кумол окисляется кислородом воздуха до гидропероксида, который при действии серной кислоты разлагается на фенол и ацетон.
Из изопропанола
По данному методу изопропанол окисляют в паровой фазе при температурах 450—650 °C на катализаторе (металлические медь, серебро, никель, платина). Ацетон с высоким выходом (до 90 %) получают на катализаторе «серебро на пемзе» или на серебряной сетке.
Метод окисления пропена
Ацетон получают также прямым окислением пропена в жидкой фазе в присутствии PdCl2 в среде растворов солей Pd, Cu, Fe при температуре 50-120 °C и давлении 50-100 атм.
Физические свойства
Ацетон — бесцветная подвижная летучая жидкость (при н.у.) с характерным резким запахом. Во всех соотношениях смешивается с водой, диэтиловым эфиром, бензолом, метанолом, этанолом, многими сложными эфирами и так далее.
Основные термодинамические свойства ацетона:
- Поверхностное натяжение (20 °C): 23,7 мН/м
- Стандартная энтальпия образования ΔH (298 К): −247,7 кДж/моль (ж)
- Стандартная энтропия образования S (298 К): 200 Дж/моль·K (ж)
- Стандартная мольная теплоемкость Cp (298 К): 125 Дж/моль·K (ж)
- Энтальпия плавления ΔHпл: 5,69 кДж/моль
- Энтальпия кипения ΔHкип: 29,1 кДж/моль
- Теплота сгорания Qp: 1829,4 кДж/моль
- Критическое давление: 4,7 МПа
- Критическая плотность: 0,273 г/см3
- Динамическая вязкость жидкостей и газов:
- 0,36 мПа·с (10 °C)
- 0,295 мПа·с (25 °C)
- 0,28 мПа·с (41 °C)
Термохимические свойства:
- Температура вспышки в воздухе: (-20 °C)
- Температура самовоспламенения на воздухе: 465 °C
- Пределы взрывоопасных концентраций: 2,6-12,8 %
Прочие свойства:
- Показатель преломления (для D-линии натрия):
- 1,3591 (20 °C)
- 1,3588 (25 °C)
- Показатель электролитической диссоциации: pKa = 20 (20 °C, вода)
- Диэлектрическая проницаемость (20 °C): 20,9
- Дипольный момент молекулы (20 °C): 2,84 Дебай
Ацетон хорошо растворяет многие органические вещества, в частности, ацетил- и нитроцеллюлозы, воски, алкалоиды и так далее, а также ряд солей.
Химические свойства
Окислительно-восстановительные реакции
Восстанавливается амальгамами магния или цинка до пинакона.
Ацетон окисляет вторичные спирты в кетоны в присутствии трет-бутилата алюминия (реакция Опенауэра).
Под действием перекиси водорода на ацетон в кислой среде образуется перекись ацетона.
Ангидрид хрома окисляет ацетон до углекислого газа и воды. Ацетон реагирует с аммиаком и водородом в присутствии никеля или меди с образованием аминов. Обычно реакция протекает при температуре 125-175 °C и давлении 5-10 атмосфер.
Присоединение нуклеофилов к карбонильной группе
Ацетон является одним из наиболее реакционноспособных кетонов. Так, он один из немногих кетонов образует бисульфитное соединение.
Ацетон легко присоединяет циановодород с образованием ацетонциангидрина.
Аналогично ацетон присоединяет хлороформ, образуя хлорэтон, который используется в качестве антисептика.
Реакции альфа-позиции
При воздействии ацетона на металлический натрий или амид натрия образуется ацетоннатрий, натриевый спирт изопропенилового спирта.
Атомы водорода в ацетоне легко замещаются на галогены. Под действием хлора (иода) в присутствии щёлочи образует хлороформ (йодоформ).
Реакции конденсации
В щелочной среде вступает в альдольную самоконденсацию, с образованием диацетонового спирта.
При конденсации трех молекул ацетона под действием концентрированной серной или соляной кислоты образуется симметричный триметилбензол (мезитилен).
Прочие реакции
При пиролизе (700 °C) образует кетен.
Применение
Ацетон применяется как сырьё для синтеза многих важных химических продуктов, таких как уксусный ангидрид, кетен, диацетоновый спирт, окись мезитила, метилизобутилкетон, метилметакрилат, дифенилпропан, изофорон, бисфенол А и так далее. Последний широко применяется при синтезе поликарбонатов, полиуретанов и эпоксидных смол.
Ацетон также является популярным растворителем. В частности он используется как растворитель
- в производстве лаков;
- в производстве взрывчатых веществ;
- в производстве лекарственных препаратов;
- в составе клея для киноплёнок как растворитель ацетата целлюлозы и целлулоида;
- компонент для очистки поверхностей в различных производственных процессах;
- как очиститель инструмента и поверхностей от монтажной пены — в аэрозольных баллонах.
Без ацетона невозможно хранить в компактном (сжиженном и в баллоне) состоянии ацетилен, который под давлением в чистом виде крайне взрывоопасен. Для этого используют ёмкости с пористым материалом, пропитанным ацетоном. 1 литр ацетона растворяет до 250 литров ацетилена.
Ацетон используется также при экстракции многих растительных веществ.
Лабораторное применение
В органической химии ацетон применяется в качестве полярного апротонного растворителя, в частности, в реакции алкилирования, для окисления спиртов в присутствии алкоголятов алюминия по Оппенауэру.
Ацетон применяется для приготовления охлаждающих бань в смеси с «сухим льдом» и жидким аммиаком (охлаждает до температуры −78 °C).
В лабораториях используется для мытья химической посуды благодаря низкой цене, малой токсичности, высокой летучести и лёгкой растворимости в воде, а также дл быстрой сушки посуды и неорганических веществ.
Пожароопасность
Одна из основных опасностей при работе с ацетоном — его легкая воспламеняемость. Температура самовоспламенения +465 °C, температура вспышки −20 °C. Воздушные смеси, содержащие от 2,5 % до 12,8 % (по объёму), взрывоопасны. С этим необходимо считаться, так как ацетон быстро испаряется, и образующееся облако может распространиться до места воспламенения (нагрев или искра) вдали от места работы с ним.
Метаболизм
Ацетон является естественным метаболитом, производимым организмами млекопитающих, в том числе и человеческим организмом. В крови в норме содержится 1—2 мг/100 мл ацетона, в суточном количестве мочи — 0,01—0,03 г. Некоторое количество ацетона превращается в оксид углерода (IV), который выделяется с выдыхаемым воздухом, некоторое — с мочой и выделениями кожи. В медицине ацетон относят к кетоновым телам. Нарушение нормального метаболизма, например, при сахарном диабете, приводит к так называемой ацетонурии — избыточному образованию и выведению ацетона.
Токсичность
Ацетон токсичен. По данным ПДК ацетона составляет 200 мг/м³ (среднесменная за 8 часов) и 800 мг/м³ (максимально-разовая). По данным ряда исследований, например средний порог восприятия запаха был в ~3 раза выше чем максимально-разовая ПДК, и в ~12 раз выше среднесменной ПДК. При этом у части работников порог был значительно выше среднего значения (например, более 30 и 120 ПДК соответственно). В исследовании среднее значение порога восприятия запаха было ещё выше — 11 000 ppm (28 000 мг/м3), что превышает среднесменную ПДК в 140 раз.
Ацетон ядовит, но относится к малоопасным веществам (класс опасности IV, категория безопасности для здоровья по NFPA — 1). Сильно раздражает слизистые оболочки: длительное вдыхание больших концентраций паров приводит к возникновению воспаления слизистых оболочек, отёку лёгких и токсической пневмонии. Пары оказывают слабое наркотическое действие, сопровождаемое, чаще всего, дисфорией. При попадании внутрь вызывает состояние опьянения, сопровождаемое слабостью и головокружением, нередко — болями в животе; в существенных количествах возникает выраженная интоксикация, хотя, как правило, отравления ацетоном не смертельны. Возможно поражение печени (токсический гепатит), почек (уменьшение диуреза, появление крови и белка в моче) и коматозное состояние. При ингаляционном воздействии ацетон выводится гораздо медленнее (в течение нескольких часов), чем поступает, и поэтому может накапливаться в организме.